सुशील जोशी [Hindi PDF, 382 kB]
डाल्टन का परमाणु सिद्धान्त एक मील का पत्थर साबित हुआ और इसके आधार पर हम रासायनिक क्रियाओं को समझ पाए। हम यह बताने में सक्षम होते गए कि किसी क्रिया में किस पदार्थ की कितनी खपत होगी। पदार्थों के सूत्र बने, परमाणु भारों के आधार पर आवर्त तालिका बनी। तत्वों के विविध गुणों को परमाणु के आधार पर समझकर हम उनको वर्गीकृत कर पाए और यह समझ पाए कि किसी पदार्थ में किस तरह के गुणधर्मों की उम्मीद करनी चाहिए। आवर्त नियम से नए तत्वों की भविष्यवाणियाँ हुईं और सही साबित हुईं। तो परमाणु सिद्धान्त की पुष्टि होती गई।
 मगर साथ-साथ एक बात और हुई। इस सिद्धान्त के कई बिन्दुओं पर पुनर्विचार भी शु डिग्री हुआ। नए-नए अवलोकनों के प्रकाश में इस सिद्धान्त में परिष्कार आवश्यक होता गया। हर बार नए अवलोकन सामने आने पर तरीका वही रहा - कुछ मान्यताएँ स्वीकार करके मूल मॉडल में सुधार किए गए या उस पर कुछ नई सीमाएँ आरोपित की गईं।
मगर साथ-साथ एक बात और हुई। इस सिद्धान्त के कई बिन्दुओं पर पुनर्विचार भी शु डिग्री हुआ। नए-नए अवलोकनों के प्रकाश में इस सिद्धान्त में परिष्कार आवश्यक होता गया। हर बार नए अवलोकन सामने आने पर तरीका वही रहा - कुछ मान्यताएँ स्वीकार करके मूल मॉडल में सुधार किए गए या उस पर कुछ नई सीमाएँ आरोपित की गईं।
जैसे इसी बात को लें कि तत्वों के बीच क्रिया क्यों होती है। क्यों कुछ तत्व क्रिया करते हैं, कुछ नहीं करते? या यह कैसे तय होता है कि वे किस अनुपात में क्रिया करेंगे? दूसरे शब्दों में, वेलेंसी यानी संयोजकता किस बात से तय होती है? क्यों हाइड्रोजन की संयोजकता 1 है जबकि कार्बन की संयोजकता 4 है? डाल्टन और उनके बाद कई सालों तक संयोजकता की अवधारणा सामने नहीं आई थी, संयोजी भार से ही काम चलता था।
विद्युत धारा से मिली राह
आगे का घटनाक्रम कई रास्तों से आगे बढ़ा। इनमें से एक महत्वपूर्ण रास्ता विद्युत धारा पर सवार था। विद्युत से मनुष्य का परिचय तो आसमान से गिरने वाली बिजली के माध्यम से काफी प्राचीन काल से था मगर ‘विद्युत क्या है’ वगैरह जैसे प्रश्न थोड़ी देर में उठे।
जब विद्युत और प्रकाश की गहराई से जाँच पड़ताल हुई तो इसके झटके परमाणु को भी लगे। देखते हैं कैसे।
दरअसल, परमाणु टूटने का रास्ता विद्युत के अध्ययन से शुरू हुआ था। आकाशीय विद्युत की बात तो अलग मगर प्राचीन काल में ही लोग यह देख चुके थे कि जब एम्बर की छड़ को किसी कपड़े या ऊन वगैरह से रगड़ा जाता है तो वह एम्बर कई चीज़ों को अपनी ओर आकर्षित करने लगता है। एम्बर को यूनानी भाषा में इलेक्ट्रिकस कहते हैं और इसी से नाम आया ‘इलेक्ट्रिसिटी’। ऐसा माना गया कि ‘इलेक्ट्रिसिटी’ नाम का एक तरल पदार्थ होता है जिसमें आकर्षण का गुण पाया जाता है।
अट्ठारहवीं सदी के शुरू में कुछ प्रयोग हुए जिनसे यह स्पष्ट हुआ कि घर्षण से पैदा होने वाला यह आकर्षण का गुण दो तरह का होता है। इसके आधार पर कुछ लोगों का मानना था कि विद्युत नामक तरल दो तरह का होता है। इसके करीब एक दशक बाद बेंजामिन फ्रेंकलिन ने सुझाया था कि दरअसल तरल तो एक ही तरह का है मगर इसके प्रभाव में भिन्नता इसलिए आती है क्योंकि इसका दबाव यानी मात्रा अलग-अलग होती है। मगर फ्रेंकलिन यह स्पष्ट नहीं कर पाए थे कि किस परिस्थिति में क्या होता है।
इस सन्दर्भ में सबसे रोचक प्रयोग विद्युत विच्छेदन से सम्बन्धित हैं। 1800 के आसपास वोल्टा ने एक विद्युत बैटरी बना ली थी। ठोस पदार्थों में विद्युत के चालक और कुचालक तो काफी पहले पहचान लिए गए थे। मगर तरल पदार्थों में विद्युत प्रवाह के प्रयोग उन्नीसवीं सदी में शुरू हुए।
पानी वैसे तो कुचालक होता है मगर यदि इसमें कोई पदार्थ घुला हो, तो कभी-कभी यह चालक की तरह व्यवहार करता है। इस तरह के कई प्रयोगों से तरल पदार्थों की चालकता को समझने में मदद मिली। इनमें से सबसे सटीक व मात्रात्मक प्रयोग माइकल फैराडे ने किए थे और ये प्रयोग व इनके निष्कर्ष परमाणु संरचना को समझने की दृष्टि से महत्वपूर्ण साबित हुए थे।
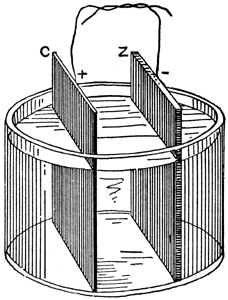
पदार्थों का विद्युत विच्छेदन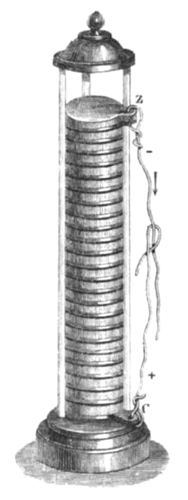 दरअसल, एलेसैंड्रो वोल्टा ने 1800 में वोल्टेइक सेल बना लिया था। इससे विद्युत धारा का एक स्रोत हाथ में आ गया। इसकी मदद से सबसे पहले हम्फ्री डेवी ने पानी में विद्युत धारा प्रवाहित की और देखा कि ऐसा करने पर पानी अपने तत्वों - हाइड्रोजन और ऑक्सीजन - में टूट जाता है। हाइड्रोजन गैस के बुलबुले ऋण इलेक्ट्रोड (कैथोड) पर तथा ऑक्सीजन के बुलबुले धन इलेक्ट्रोड (एनोड) पर इकट्ठे होते हैं। इस क्रिया को विद्युत विच्छेदन कहते हैं। हम्फ्री डेवी ने कई पदार्थों का विद्युत विच्छेदन करके देखा था। जब उन्होंने हाइड्रोक्लोरिक अम्ल (उस समय उसे म्यूरिएटिक एसिड कहते थे) में विद्युत प्रवाहित की तो कैथोड पर हाइड्रोजन और एनोड पर एक नई गैस मुक्त हुई। इस नई गैस को क्लोरीन नाम दिया था। इसी विधि से उन्होंने सोडियम व पोटेशियम तत्वों की भी खोज की थी।
दरअसल, एलेसैंड्रो वोल्टा ने 1800 में वोल्टेइक सेल बना लिया था। इससे विद्युत धारा का एक स्रोत हाथ में आ गया। इसकी मदद से सबसे पहले हम्फ्री डेवी ने पानी में विद्युत धारा प्रवाहित की और देखा कि ऐसा करने पर पानी अपने तत्वों - हाइड्रोजन और ऑक्सीजन - में टूट जाता है। हाइड्रोजन गैस के बुलबुले ऋण इलेक्ट्रोड (कैथोड) पर तथा ऑक्सीजन के बुलबुले धन इलेक्ट्रोड (एनोड) पर इकट्ठे होते हैं। इस क्रिया को विद्युत विच्छेदन कहते हैं। हम्फ्री डेवी ने कई पदार्थों का विद्युत विच्छेदन करके देखा था। जब उन्होंने हाइड्रोक्लोरिक अम्ल (उस समय उसे म्यूरिएटिक एसिड कहते थे) में विद्युत प्रवाहित की तो कैथोड पर हाइड्रोजन और एनोड पर एक नई गैस मुक्त हुई। इस नई गैस को क्लोरीन नाम दिया था। इसी विधि से उन्होंने सोडियम व पोटेशियम तत्वों की भी खोज की थी।
अलबत्ता, विद्युत विच्छेदन के साथ गहनता से मात्रात्मक प्रयोग माइकल फैराडे ने 1833 में किए थे। जैसे, फैराडे ने पानी का विद्युत विच्छेदन करते समय हाइड्रोजन व ऑक्सीजन की मात्रा को नापा। फिर उन्होंने इन मात्राओं और विद्युत धारा के बीच सम्बन्ध देखने की कोशिश की। उन्होंने पाया कि हर इकाई बिजली बहने पर हाइड्रोजन के दो इकाई आयतन और ऑक्सीजन का एक इकाई आयतन बनता है। यदि विद्युत की मात्रा दुगनी कर दी जाए, तो दोनों गैसों की मात्रा भी दुगनी हो जाती है।
इसी प्रकार से उन्होंने यह भी नापा कि जब कॉपर सल्फेट के घोल का विद्युत विच्छेदन करते हैं, तो कैथोड पर जमा होने वाले ताँबे की मात्रा विद्युत की मात्रा के समानुपाती होती है।
पानी के विद्युत विच्छेदन से हाइड्रोजन व ऑक्सीजन बनने के मामले में यह भी स्पष्ट था कि हाइड्रोजन का आयतन हमेशा ऑक्सीजन से दुगना होता था। वज़न के हिसाब से देखेंगे तो एक इकाई विद्युत से यदि 1.008 ग्राम हाइड्रोजन पैदा होगी तो ऑक्सीजन 8 ग्राम। इन मात्राओं का सम्बन्ध इन गैसों के परमाणु भारों से है। जहाँ हाइड्रोजन अपने परमाणु भार के बराबर बनती है वहीं ऑक्सीजन अपने परमाणु भार से आधी।
जब फैराडे ने नमक को पिघलाकर उसका विद्युत विच्छेदन किया तो कैथोड पर सोडियम और एनोड पर क्लोरीन गैस जमा हुई। एक कूलंब आवेश प्रवाहित होने पर 2.38न्10-4 ग्राम सोडियम और 3.68न्10-4 ग्राम क्लोरीन मिली। इसका मतलब हुआ कि 1 ग्राम परमाणु भार सोडियम (23 ग्राम) जमा करने के लिए 96,500 कूलंब विद्युत प्रवाहित करनी होगी। इसी प्रकार से 1 ग्राम परमाणु भार क्लोरीन (35.5 ग्राम) प्राप्त करने के लिए भी 96,500 कूलंब आवेश प्रवाहित करना होगा।
इसी प्रकार से यदि पानी में 96,500 कूलंब विद्युत प्रवाहित की जाए, तो 1.0008 ग्राम हाइड्रोजन (1 ग्राम-परमाणु भार) और 8 ग्राम (यानी आधा ग्राम-परमाणु भार) ऑक्सीजन हासिल होगी। ग्राम परमाणु भार से आशय है उस तत्व का परमाणु भार ग्राम में व्यक्त करना।
कुल मिलाकर फैराडे के इन नपे-तुले प्रयोगों से दो नियम उभरे। पहला नियम यह था कि विद्युत विच्छेदन के दौरान किसी भी पदार्थ की मुक्त मात्रा कुल विद्युत धारा की मात्रा के समानुपाती होती है। और दूसरा नियम कि तत्व की मुक्त मात्रा उसके ग्राम परमाणु भार बटा संयोजकता के भी समानुपाती होती है। इन नियमों की व्याख्या कैसे हो? एक तो परमाणु सिद्धान्त के मुताबिक पदार्थ परमाणु से बने होते हैं। इसलिए विद्युत विच्छेदन के दौरान उनका परमाणु भारों के अनुपात में पैदा होना परमाणु के अस्तित्व की पुष्टि करता है।
इन नियमों की व्याख्या कैसे हो? एक तो परमाणु सिद्धान्त के मुताबिक पदार्थ परमाणु से बने होते हैं। इसलिए विद्युत विच्छेदन के दौरान उनका परमाणु भारों के अनुपात में पैदा होना परमाणु के अस्तित्व की पुष्टि करता है।
मगर इन मात्राओं का विद्युत की मात्रा के समानुपाती होने की बात का क्या अर्थ है? इससे भी ज़्यादा महत्वपूर्ण बात तो यह है कि विद्युत की एक निश्चित मात्रा के प्रभाव स्वरूप हरेक तत्व की जो मात्रा एकत्रित होती है वह उसके परमाणु भार में संयोजकता का भाग देने से प्राप्त मान के समानुपाती होती है। इसका मतलब यह निकाला जा सकता है कि विद्युत भी कुछ बुनियादी न्यूनतम मात्राओं के रूप में पाई जाती है और विद्युत की यह न्यूनतम मात्रा विद्युत के एक परमाणु के रूप में व्यवहार करती है। फैराडे के नियमों के आधार पर विद्युत की इस न्यूनतम मात्रा की गणना की गई थी जो एक-संयोजी आयन के आवेश के बराबर थी।
इस बात पर फैराडे ने विचार ज़रूर किया था मगर वे परमाणु के अस्तित्व को लेकर ही आश्वस्त नहीं थे। इसलिए उन्होंने इस विचार को ज़्यादा तरजीह नहीं दी।
|
विद्युत अपघटन विद्युत विच्छेदन या विद्युत अपघटन के प्रयोग सबसे पहले हम्फ्री डेवी ने किए थे और पिघले नमक (सोडियम क्लोराइड) में विद्युत प्रवाहित करके सोडियम व क्लोरीन प्राप्त की थी। कतिपय तरल पदार्थों में विद्युत प्रवाहित करने पर उनका अपघटन हो जाता है और उनके हिस्से इलेक्ट्रोड्स पर मुक्त हो जाते हैं। |
 वैसे उस समय तक अर्हीनियस आयन सिद्धान्त का प्रतिपादन कर चुके थे। यदि हम यह मानें कि विद्युत विच्छेदन के दौरान आवेश आयनों पर सवार होकर गमन करते हैं, तो ज़ाहिर है कि आवेश की एक न्यूनतम मात्रा होनी चाहिए जो एक आयन के साथ सम्बद्ध होगी। कुल मिलाकर निष्कर्ष यह था कि पदार्थ के परमाणु के समान विद्युत की भी एक निश्चित न्यूनतम मात्रा या इकाई होती है। 1838 में रिचर्ड लैमिंग ने परमाणुओं के रासायनिक गुणधर्मों की व्याख्या के लिए यह सुझाव रखा था कि विद्युत की एक अविभाज्य मात्रा (इकाई) होती है। लैमिंग ने तो यहाँ तक कयास लगाया था कि परमाणु में एक केन्द्रीय भाग (कोर) होता है जिसके आसपास कुछ उप-परमाण्विक कण उपस्थित होते हैं जो इकाई विद्युत आवेश के वाहक होते हैं। फैराडे के विद्युत विच्छेदन के नियमों का गहराई से अध्ययन करके एक अन्य भौतिक शास्त्री जॉर्ज जॉनस्टोन स्टोनी ने सुझाव दिया था कि विद्युत की एक निश्चित न्यूनतम मात्रा होती है जो एक एक-संयोजी आयन के बराबर होती है। वे इस बुनियादी आवेश के मान का हिसाब लगाने में भी सफल रहे थे। दरअसल, इलेक्ट्रॉन शब्द स्टोनी ने ही 1891 में दिया था। उनके मुताबिक, “विद्युत की इस बुनियादी मात्रा का अनुमान लगाने के बाद मैंने इसे इलेक्ट्रॉन नाम दिया है।
वैसे उस समय तक अर्हीनियस आयन सिद्धान्त का प्रतिपादन कर चुके थे। यदि हम यह मानें कि विद्युत विच्छेदन के दौरान आवेश आयनों पर सवार होकर गमन करते हैं, तो ज़ाहिर है कि आवेश की एक न्यूनतम मात्रा होनी चाहिए जो एक आयन के साथ सम्बद्ध होगी। कुल मिलाकर निष्कर्ष यह था कि पदार्थ के परमाणु के समान विद्युत की भी एक निश्चित न्यूनतम मात्रा या इकाई होती है। 1838 में रिचर्ड लैमिंग ने परमाणुओं के रासायनिक गुणधर्मों की व्याख्या के लिए यह सुझाव रखा था कि विद्युत की एक अविभाज्य मात्रा (इकाई) होती है। लैमिंग ने तो यहाँ तक कयास लगाया था कि परमाणु में एक केन्द्रीय भाग (कोर) होता है जिसके आसपास कुछ उप-परमाण्विक कण उपस्थित होते हैं जो इकाई विद्युत आवेश के वाहक होते हैं। फैराडे के विद्युत विच्छेदन के नियमों का गहराई से अध्ययन करके एक अन्य भौतिक शास्त्री जॉर्ज जॉनस्टोन स्टोनी ने सुझाव दिया था कि विद्युत की एक निश्चित न्यूनतम मात्रा होती है जो एक एक-संयोजी आयन के बराबर होती है। वे इस बुनियादी आवेश के मान का हिसाब लगाने में भी सफल रहे थे। दरअसल, इलेक्ट्रॉन शब्द स्टोनी ने ही 1891 में दिया था। उनके मुताबिक, “विद्युत की इस बुनियादी मात्रा का अनुमान लगाने के बाद मैंने इसे इलेक्ट्रॉन नाम दिया है।
अलबत्ता इस विचार (विद्युत की परमाणु प्रकृति) को उन्नीसवीं सदी के अन्त तक मान्यता नहीं मिली।
 गैस व कैथोड किरणें
गैस व कैथोड किरणें
तरल पदार्थों की विद्युत चालकता के अध्ययन के बाद नम्बर आया गैसों का। गैसों की चालकता के अध्ययन का तरीका यह था कि किसी नली में गैस को भर लें। नली के एक सिरे पर कैथोड और दूसरे सिरे पर एनोड लगा दें। फिर उन दो इलेक्ट्रोड के बीच ज़ोरदार विभवान्तर पैदा करें और देखें कि क्या होता है। इस प्रयोग के परिणामों का अवलोकन करने के लिए अच्छा होता है कि नली में गैस का दबाव कम हो।
सबसे पहले गैसों की चालकता से सम्बन्धित प्रयोग जर्मन भौतिक शास्त्री जोहान विल्हेल्म हिटॉफ ने किए थे। 1869 में उन्होंने देखा कि जब कम दबाव पर गैस भरी नली में विद्युत प्रवाहित की जाती है तो कैथोड से एक चमक निकलती है। उन्होंने यह भी देखा कि यदि गैस का दबाव और कम किया जाए, तो यह चमक बढ़ती है।
इस चमक की किरणों पर आगे प्रयोग करने पर देखा गया कि यदि इसके रास्ते में कोई चीज़ रख दी जाए तो उसकी छाया बनती है। जर्मन भौतिक शास्त्री यूजेन गोल्डस्टाइन ने इन किरणों को कैथोड किरण नाम दिया।
अब तो कई वैज्ञानिकों की रुचि इन कैथोड किरणों के अध्ययन में पैदा हो चुकी थी। विलियम क्रुक्स ने ऐसी ही कैथोड किरण नली बनाई जिसमें अच्छा खासा निर्वात पैदा किया जा सकता था। इस नली में प्रयोग करके वे यह दर्शाने में सफल रहे थे कि ये किरणें कैथोड से एनोड की ओर जाती हैं और इनमें ऊर्जा होती है। सबसे बड़ी बात तो वे यह दर्शा पाए कि यदि इन किरणों को एक चुम्बकीय क्षेत्र में से गुज़ारा जाए, तो ये अपने मार्ग से विचलित हो जाती हैं। विचलन की दिशा के आधार पर वे यह भी दर्शा पाए थे कि ये किरणें ऋणावेशित होती हैं।
कैथोड किरणों के उपरोक्त गुणधर्मों की व्याख्या के लिए उन्होंने यह माना कि ये किरणें पदार्थ का एक नया रूप हैं - विकिरित पदार्थ। उनके मुताबिक ये किरणें दरअसल ऋणावेशित अणुओं से बनी थीं जो कैथोड में से तेज़ गति से निकलते हैं।
ऋण आवेश वाले कण - इलेक्ट्रॉन क्रुक्स ने कैथोड किरणों को चुम्बकीय क्षेत्र में विचलित करके देखा था। एक अन्य वैज्ञानिक आर्थर शूस्टर ने किरणों के मार्ग के दोनों ओर एक-एक धातुई प्लेट लगाई और उन दोनों के बीच विभवान्तर पैदा किया। जब कैथोड किरणें इन प्लेट्स के बीच से गुज़रीं तो वे धनात्मक प्लेट की ओर मुड़ गईं। इससे पक्का हो गया कि कैथोड किरणें ऋणात्मक आवेश वाली हैं। मगर शूस्टर एक कदम आगे बढ़े। विचलन की मात्रा के आधार पर वे किरणों के घटकों के आवेश और द्रव्यमान के अनुपात की गणना कर पाए। मगर उनकी गणनाओं से जो मान निकला वह अपेक्षा से इतना ज़्यादा था कि उनके गणना के तरीके पर ही सवाल उठ गए।
क्रुक्स ने कैथोड किरणों को चुम्बकीय क्षेत्र में विचलित करके देखा था। एक अन्य वैज्ञानिक आर्थर शूस्टर ने किरणों के मार्ग के दोनों ओर एक-एक धातुई प्लेट लगाई और उन दोनों के बीच विभवान्तर पैदा किया। जब कैथोड किरणें इन प्लेट्स के बीच से गुज़रीं तो वे धनात्मक प्लेट की ओर मुड़ गईं। इससे पक्का हो गया कि कैथोड किरणें ऋणात्मक आवेश वाली हैं। मगर शूस्टर एक कदम आगे बढ़े। विचलन की मात्रा के आधार पर वे किरणों के घटकों के आवेश और द्रव्यमान के अनुपात की गणना कर पाए। मगर उनकी गणनाओं से जो मान निकला वह अपेक्षा से इतना ज़्यादा था कि उनके गणना के तरीके पर ही सवाल उठ गए।
मगर इतना स्पष्ट था कि इन किरणों के घटकों में द्रव्यमान होता है। अर्थात् ये कण हैं। अन्तत: जे.जे. थॉमसन, जॉन टाउनसेंड और एच.ए. विल्सन ने मिलकर 1896 में वे ऐतिहासिक प्रयोग किए जिनकी मदद से इलेक्ट्रॉन की खोज हो पाई।
थॉमसन कुछ निहायत नफीस प्रयोगों और तर्क की मदद से इन कणों के आवेश और द्रव्यमान, दोनों की गणना कर पाए थे। फैराडे के विद्युत विच्छेदन के प्रयोगों से एक बात और स्पष्ट हो चुकी थी। सबसे हल्का आवेशित कण हाइड्रोजन का आयन पाया गया था। जब थॉमसन ने कैथोड किरण कणों (जिन्हें वे कार्पस्कल कहते थे) के द्रव्यमान की गणना की तो पता चला कि ये कार्पस्कल उस सबसे हल्के आवेशित कण से भी करीब 2000 गुना हल्के थे। थॉमसन द्वारा किए गए प्रयोगों का ज़िक्र थोड़ी देर बाद करेंगे। पहले उनके परिणामों और उन परिणामों के आधार पर निकाले गए निष्कर्षों को देख लेते हैं।
उन्होंने कैथोड किरण नली (जिसे अब क्रुक्स नलिका कहने लगे थे) में कैथोड बनाने के लिए कई पदार्थों का उपयोग किया था। परिणाम यह रहा कि कैथोड किसी भी पदार्थ का बना हो, कैथोड-कार्पस्कल का आवेश-द्रव्यमान अनुपात वही रहता है। यानी कैथोड-कार्पस्कल कैथोड की सामग्री से स्वतंत्र हैं। यह भी देखा गया कि नलिका में कोई भी गैस भरें, इन कार्पस्कल की प्रकृति (द्रव्यमान-आवेश अनुपात) एक जैसा ही रहता है। इसके आधार पर थॉमसन का निष्कर्ष था कि ये कार्पस्कल किसी भी परमाणु के बुनियादी घटक हैं।
थॉमसन यह भी दर्शा पाए कि रेडियोधर्मी पदार्थों से या पदार्थों को गर्म करने पर या पदार्थों को प्रकाशित करने पर जो ऋणावेशित कण निकलते हैं वे एक जैसे होते हैं। इन कणों को इलेक्ट्रॉन नाम दिया गया।

कैथोड ट्यूब से प्रयोग: जे.जे. थॉमसन ने कैथोड किरणों के साथ प्रयोग में मिले अवलोकनों के आधार पर बताया कि कैथोड किरणें ऋणात्मक आवेश वाले कणों से बनी किरणें हैं जो आकार में परमाणु से छोटी हैं। बाद में इन कणों को इलेक्ट्रॉन नाम दिया गया।
तो इन विभिन्न प्रयोगों से यह स्पष्ट हो गया कि परमाणु अविभाज्य नहीं बल्कि इसमें इलेक्ट्रॉन नामक कण पाए जाते हैं, जो कुछ परिस्थितियों में अलग हो जाते हैं। इन कणों का आवेश ऋणात्मक और द्रव्यमान सबसे हल्के आयन (हाइड्रोजन आयन) से 2 हज़ार गुना कम पाया गया।
यानी थॉमसन के प्रयोगों ने करीब 200 सालों से अविभाज्य माने जा रहे परमाणु को तोड़ दिया था। और ऐसा लग रहा था कि परमाणु स्वयं कुछ कणों से मिलकर बना है और ये कण सारे परमाणुओं में एक जैसे हैं। यानी अब हम परमाणु से उप-परमाण्विक कणों की दुनिया में प्रवेश कर चुके थे।
समस्या यह है कि परमाणु तो विद्युतीय दृष्टि से उदासीन होता है और जो कण उसमें से निकल रहे हैं, वे ऋणावेशित हैं। मतलब यह हुआ कि इन्हें सन्तुलित करने के लिए कोई धनावेश भी होना चाहिए।
ऋण और धन आवेश का मॉडल
1897 में इलेक्ट्रॉन की खोज के बाद थॉमसन ने अटकल का सहारा लिया। धनावेश युक्त कोई कण तो मिला नहीं था। तो थॉमसन ने परमाणु संरचना का जो मॉडल प्रस्तुत किया उसमें उपलब्ध जानकारी का अच्छा समावेश था। उन्होंने कहा कि परमाणु में एक धनावेश का बादल-सा रहता है। और ऋणावेशित कण इस बादल में यहाँ-वहाँ धँसे होते हैं। इसे परमाणु संरचना का तरबूज़ मॉडल कह सकते हैं, वैसे पाठ्य पुस्तकों ने आम तौर पर इसे ‘प्लम पुडिंग’ मॉडल नाम दिया है। इस मॉडल में तरबूज़ का लाल-लाल हिस्सा तो धनावेश का फैलाव है और जो काले-काले बीज उसमें नज़र आते हैं, वे इलेक्ट्रॉन हैं।
जहाँ एक ओर कैथोड किरणों की खोज हुई, वहीं यूजेन गोल्डस्टाइन ने एक अन्य किरण की खोज कर डाली। 1886 में गोल्डस्टाइन ने कैनाल किरणों की खोज की जिन्हें एनोड किरणें भी कहते हैं। ये कैनाल किरणें भी आवेशित कणों से बनी थीं और गैसों के आयनीकरण से पैदा होती थीं। मगर देखा गया कि अलग-अलग गैसों से उत्पन्न एनोड किरण कणों का आवेश-द्रव्यमान अनुपात अलग-अलग था। अर्थात् इन्हें किसी एक कण से बना नहीं माना जा सकता था, जैसा कि कैथोड किरणों के बारे में मानना सम्भव था।
यदि धनावेशित कण नहीं हैं तो यही एक तरीका हो सकता है जिससे इलेक्ट्रॉन युक्त परमाणु उदासीन रह सकता है। मगर धनावेशित कणों की खोज ज़्यादा दूर नहीं थी। इन्हीं धनावेशित कणों की खोज परमाणु संरचना का अगला कदम होगा।
(...जारी )
सुशील जोशी: एकलव्य द्वारा संचालित स्रोत फीचर सेवा से जुड़े हैं। विज्ञान शिक्षण व लेखन में गहरी रुचि।