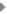सुशील जोशी
. . . और सहबंध बनने की प्रक्रिया मे एकपरमाणु का नाभिक दूसरे के इलेक्टॉन बादल को आकर्षित करता है, वहीं समान आवेश के कारण दोनों के नाभिक कए दूसरे को विकर्षित करने लगते हैं . . . सहबंध दरअसल वह दूरी है जिस पर आकर्षण और विकर्षण बलों में संतुलन बना हुआ है।
यह बात समझना काफी आसान है कि किसी भी वजह से यदि एक परमाणु ऋणावेशित हो और दूसरा धनावेशित, तो उनके बीच आकर्षण होगा तथा वे परस्पर जुड़े रहेंगे। यह समझना आसान इसलिए है क्योंकि यह बात हमारे स्थूल अनुभवों-अवलोकनों से मेल खाती है। मगर जब हम इस बात पर विचार करें कि क्यों कई अधातुएं (खासकर गैसें) एक ही किस्म के दो-दो परमाणुओं के जोड़ों के रूप में रहती हैं- तो स्थिति पेचीदा हो जाती है। इनमें विद्युतीय आकर्षण का कोई कारण नज़र नहीं आता। समलन ऑक्सीजन(O2), हाइडोजन(H2), जाइटोजन(N2), क्लोरीन(CL2), ब्रोमीन(Br2), वगैरह अधात्विक तत्व द्विपरमाण्विक रूप में ही आमतौर पर पाए जाते हैं। सवाला यह उठता है कि ऐसा क्यों है। इसके साथ ही यह सवाल भी है कि कई सारे तत्व ऐसे भी हैं जिनमें आयन निर्माण, ऊर्जा की दृष्टि से इतना आसान नहीं है। फिर इनमें यैगिक निर्माण क्यों कर होता है। ऐतिहासिक रूप से इस सम्बंध मे कई व्याख्याएं प्रस्तुत की गईं। यहां हम उन सारी व्याख्याओं में नहीं जा रहे हैं मगर उनको पढ़कर दो बातें स्पष्ट रूप से ज़ाहिर होती हैं। पहली बात तो यह कि रसायनज्ञ इस तरह के द्विपरमाण्विक तत्वों व गैर आयनिक यौगिकों की व्याख्या के लिए हाथ- पांव मार रहे थे अौर उस समय उपलब्ध जानकारी व धारणओं की सीमाओं में भसक प्रयत्न कर रहे थे। दूसरी बात यह ज़ाहिर होती है कि उस समय विकसित धारणाओं की सीमाएं एक वड़ी बाधा बन चुकी थीं।
खैर, थोड़ा आधुनिक युग की ओर बढ़रें तो सामने आते हैं- परमाणु संबंधी ‘लुईस का मॉडल’।
बोर के मॉडल की मुख्य बात यह है कि इसमे माना गया था कि परमाणु का सारा धनात्मक आवेश केनद्र में घनीभूत है और इलेक्टॉन इस केन्द्रक के इर्द-गिर्द चक्कर काटते रहते हैं। इसमें एक प्रमुख बात यह थी कि इलेक्टॉनों के चक्कर काटने के कुछ नियम प्रतिपादित किए गए थे। इनमें से एक प्रमुख नियम यह था कि इलेक्टॉन चनद निर्धरित ऊर्जा स्तरों पर चक्कर काटते हैं; और ये इलेक्टॉन एक ऊर्जा स्तर से किसी दूसरे निश्चित ऊर्जा स्तर पर ही जाएंगे। इन ऊर्जा स्तरों को इलेक्टॉन कक्षा(Orbit) कहा गया।
इस मॉडल का अर्थ यह है कि ये इलेक्टॉन एक ऊर्जा स्तर से दूसरे ऊर्जा स्तर पर पहुंचने के लिए या तो एक निश्चित मात्रा में ऊर्जा सोखेंगे या उत्सर्जित करेंगे। इससे कम-ज्यादा ऊर्जा मिलने पर यह स्तर-परिवर्तन नहीं होगा। यानी ऊर्जा क्वांटम के रूप मे ही चाहिए।
इन विभिन्न ऊर्जा स्तरों को s, p, d, f, वगैरह के नाम से जानते हैं। प्रत्येक स्तर मे फिर उपस्तर होते हैं तथा उपस्तरों में फिर और उप-उप स्तर होते हैं। इस तरह से किसी परमाणु में किसी भी इलेक्टॉन की स्थिति की पहचान के लिए चार क्वांटम संख्याएं निर्धारित की गई हैं।
वैसे यह एक बहुत स्थूल चित्र है तथा बारीकियों को छोड़कर बताया गया है।
बहरहाल इसके आधार पर लुईस के मॉडल को समझा जा सकता है। लुईस ने 1916 में यह मॉडल प्रस्तावित किया था। तब से लेकर आज तक के अंतराल के दौरान रासायनिक बन्धनों की हमारी समझ में काफी वृद्धि हुई है। मगर प्रस्तुतीकरण के लिहाज़ से आज भी लुईस का मॉडल उपयोगी है तथा उपयोग किया जाता है।
साझा इलेक्टॉन और बंध
लुईस ने अपने मॉडल का आधार दो बातों को बनाया था:
1. सामान्यत: किसी भी परमाणु की सबसे बाहरी कक्षा मे उपस्थित इलेक्टॉन ही रासायनिक बधंन मे भाग लेते हैं। इन्हें दर्शाने के लिए लुर्ठस ने एक परिपाटी विकसित की। तत्व के संके के चारों ओर इन इलेक्टॉनों को बिन्दुओं के रूप में दर्शाया जाता है:
H. He: .B: C. N O F Ne
इन्हें बन्धनक्षम (वेलेन्स) इलेक्टॉन कहा जाता है।
2. लुईस ने यह विचार रखा कि प्रत्येक तत्व अक्रिय (नोबल) गैसों के समान इलेक्टॉन संरचना हासिल करने के लिए रासायनिक बंधन बताना है। यह इलेक्टॉन संरचना दो तरह से हासिल की जा सकती है;
Na (2,8,1) Na+ (2,8)
F (2,7) F (2,8)
अगर सरल शब्दों में इसे देखें तो इसका मतलब है कि यदि सोडियम परमाणु अपना एक इलेक्टॉन फ्लोरीन परमाणु को दे दे तो दोनों को इलेक्टॉन संरचना नोबल गैस नियॉन जैसी हो जाएगी। इस तरह के आयनिक बन्धन की चर्चा संदर्भ के पिछले अंक में की गई थी। नोबल गैस संरचना हासिल करने का एक तरीका यह भी है कि दोनों परमाणु एक-एक इलेक्टॉन की साझेदारी करें:
H + I H I
साझा इलेक्टॉन अब दोनों परमाणुओं के लिए नोबल गैस संरचना निर्मित करने का काम करते हैं। लिहाजा यह अणु बनकर सथायित्व प्राप्त करता है। इलेक्टॉनों की साझेदारी से बने बन्धन को सहबन्ध कहते हैं। इसे चाहें तो उन एक आड़ी लाईन द्वारा भी:
H + H H : H H - H
F + F F + F F: F F-F
आप देश सकते हैं कि फ्लोरीन परमाणु में साझा इलेक्टॉन के अलावा बन्धनक्षम स्तर पर तीन जोड़ी इलेक्टॉन और है। कर्ज- इलेक्टॉन जोड़ी कहा जाता है।
लुईस के मॉडल के मुताबिक इ
स तरह इलेक्टॉन साझेदारी के फलस्वरूप दोनों परमाणुओं को जो नोबल गैस संरचना हासिल होती है वह इस पूरी इकाई की ऊर्जा को कम कर देती है।
लिहाजा स्वतंत्र परमाणुओ की तुलना में यह अणु ज़्यादा टिकाऊ होता है। इस अणु के दोनो परमाणओं के एक दूसरे से पृथक करने के लिए जितनी ऊर्जा खर्च करना होगी, उसे बन्धन ऊर्जा कहते हैं। H2 की बन्धन ऊर्जा 103 किलो कैलोरी प्रति मोल है जबकि F2 की बन्धन ऊर्जा 36 किलो कैलोरी प्रति मोल है। यानी H2 की तुलना में F2 ज़्यादा अस्थिर अणु है।
परमाणु से अणु बनने की इस प्रक्रिया में एक-एक इलेक्टॉन की ही साझेदारी हो, ऐसा ज़रूरी नहीं है। दो-दो या तीन-तीन इलेक्टॉनों की साझेदारी भी हो सकतह है:
इन्हें हम दोहरा बन्ध या तिहरा बन्ध कह सकते हैं। वैसे पाठ्य-पुस्तकें शायद एक बन्ध, द्विबन्ध और त्रिबन्ध शब्दों का प्रयो करती हैं। जाहिर है कि जितने ज़्यादा इलेक्टॉनों की साझेदारी होगी, बन्धन उतना ही मज़बूत होगा। F2 की बन्धन ऊर्जा 36 किलो कैलोरी प्रति मोल है जबकि O2की 118 और N2 की 225 किलो कैलोरी प्रति मोल है।
कुल मिलाकर लुईस के मॉडल ने नोबल गैस संरचना की स्थिरता के आधार पर गैर-आयनिक बन्धनों के बनने की एक अच्छी व्याख्या प्रस्तुत की।
अधिकतम संभावना ऑर्बिटल में
मगर मात्र इतना कह देना कि इलेक्ट्रॉन की साझे दारी से तंत्र की ऊर्जा कम हो जाती है, पर्याप्त नहीं लगता। आखिर ऊर्जा कम क्यों हो जाती है? यानी ऐसी स्थिति में इन परमाणुओं को अलग-अलग करना क्यों मुश्किल होता है? इन बातों को समझने के लिए दो सिद्धांत या मॉडल प्रस्तुत किए गए हैं। इन्हें हम ‘वेलेन्स बॉण्ड मॉडल’ तथा ‘मॉलिक्यूलर ऑर्बिटल मॉडल’ के नाम से जानते हैं। इन मॉडल्स को समझने से पहले एक-दो बातें स्पष्ट कर लेना आवश्यक है।
S, 2p और 3d ऑर्बिटल की आकृतियां। s आर्बिटल गेंदनुमा होता है, 2p ऑर्बिटल डमरू के आकार का और 3d ऑर्बिटल, दो डमरू आपस में गुंथे हुए हों इस तरह की। ये सारी आकृतियां त्रिआयामी हैं।
2. तीन 2p ऑर्बिटल: px, py, pz और नीचे pz कक्षा का इलेक्ट्रॉन घनत्व मानचित्र।
3. जो छोटा गोला है उसकमें इलेक्ट्रॉन के पाए जाने की संभाविता 50 प्रतिशत है और बाहरी घेरे के भीतर इलेक्ट्रॉन पाए जाने की संभाविता 90 फीसदी है।
पांच 3d ऑर्बिटल:dxy, dxz, dx2, dx2-y2
पहली बात कि ये मॉडल क्वांटम यांत्रिकी की धारणाओं पर आधारित हैं। इसका मतलब यह है कि इलेक्ट्रॉन को एक कण न मानकर कण व तरंग का मिला-जुला रूप माना जाता है। कई कारणों से हम यह भी नहीं बता सकते कि किसी एक क्षण पर यह इलेक्ट्रॉन ठीक-ठीक कहां है। अत: हम इस बात की गणना करते हैं कि किसी दिए गए स्थान (आयतन) में इसके होने की संभाविता कितनी है। अधिकतम सम्भाविता वाला क्षेत्र ‘ऑर्बिटल’ कहलाता है। मतलब यह नहं कहा जा रहा है कि इसके अलावा कहीं ओर इस इलेक्ट्रॉन के पाए जाने की सम्भाविता शून्य है। कहा यह जा रहा है कि ऑर्बिटल क्षेत्र के बाहर सके पाए जाने की सम्भाविता नगण्य है।
प्रत्येक ऑर्बिटल का अपना एक आकार है। हमने ऊपर s, p, d, f ऑर्बिटल की बात की थी। इनकी आकृतियां त्रि में देखिए। कई बार ऑर्बिटल के अलग-अलग हिस्सों पर धन व ऋण के चिन्ह लगाए जाते हैं। इन चिन्हों का विद्युत आवेश से कुछ लेना-देना नहीं है। जब किसी भी इलेक्ट्रॉन तरंग के क्वांटम यांत्रिकी समीकरण का विश्लेषण किया जाता है तो उसके दो समाधान मिलते हैं। इनमें से एक का चिन्ह धन होता है तथा दूसरे का ऋण होता है। ऑर्बिटल के चिन्ह वही चिन्ह हैं।
बोर के परमाणु मॉडल में जिन कक्षाओं यानी ऑर्बिट की बात की गई थी उनसे ये ऑर्बिटल एक खास अर्थ में अलग हैं। ऑर्बिट या कक्षा लगीाग उस तरह की बात है जैसे कि हम पृथ्वी की कक्षा की बात करते है। इसमें (या यों कहें कि इस पर) पृविी चक्कर लगाती है। यह एक प्रकार से एक रास्ते का घोतक है। इलेक्ट्रॉन और ऑर्बिटल का मामला इससे थोड़ा अलग है। चाहे हम ऑर्बिटल को एक रेखा द्वारा चित्रित करें मगर उसका अर्थ यह है कि उस रेखा (वास्तव में सतह) द्वारा घेरे गए आयतन के अन्दर इलेक्ट्रॉन के होने की सम्भाविता निश्चित है व काफी ज़्यादा है।
इस सम्भाविता के आधार पर हम विभिन्न स्थानों पर इलेक्ट्रॉन घनत्व की गणना भ कर सकते हैं। इसे दर्शाने के कई तरीके हैं। एक तरीका इलेक्ट्रॉन बादल(electron cloud) का है। इसमें किसी निश्चित आयतन को बारीक-बारीक बिन्दुओं से बने एक बादल के रूप में दर्शाया जाता है। इसका तात्पर्य सिर्फ इतना है कि जहां बिन्दुओं का घनत्व ज़्यादा है वहां इलेक्ट्रॉन के होने की सम्भाविता ज़्यादा है मतलब इलेक्ट्रॉन घनत्व अधिक है। इसी चीज़ को दर्शाने का एक तरीका यह भी है कि हम कि हम व्यावहारिक दृष्टि से अधिकतम घनत्व वाले क्षेत्र को एक रेखा से घेर दें। इसी प्रकार का एक विकसित रूप है- इलेक्ट्रॉन घनत्व मानचित्र। इसमें उन स्थानों को एक रेखा द्वारा जोड़ दिया जाता है जहां इलेक्ट्रॉन घनत्व एक-सा हो। इस तरह के विभिन्न प्रस्तुतीकरण चित्र में देखिए।
आकर्षण भी, विकर्षण भी
अब देखते है कि सहबन्धन का आशय क्या है। मान लीजिए हम हाइड्रोजन के दो परमाणुओं से हाइड्रोजन का अणु बनने का उदाहरण लेते हैं। प्रत्येक परमाणु को से दर्शाया जा सकता है। जब ये दो परमाणु एक-दूसरे से अनन्त दूरी पर हों, तो ये एक-दूसरे पर कोई प्रभाव नहीं डालेंगे। इस स्थिति में इनकी अपनी-अपनी स्वतंत्र इलेक्ट्रॉनिक संरचना होगी। हाइड्रोजन परमाणु में एक ही इलेक्ट्रॉन है तथा यह 1 ऑर्बिटल में रहता है। इस ऑर्बिटल की बनावट एक गेंद के समान मान सकते हैं। यानी केन्द्रक के आसपास चारों ओर इलेक्ट्रॉन घनत्व समान रूप से वितरित होता है। यह एक सुडौल ऑर्बिटल है। इस अवस्था में प्रत्येक परमाणु की एक निश्चित ऊर्जा होगी।
1 (अ)2p ऑर्बिटल में इलेक्ट्रॉन पाए जाने की संभाविता दर्शाने का एक और तरीका- बिन्दुओं का घनत्व संभाविता प्रदर्शित करता है।
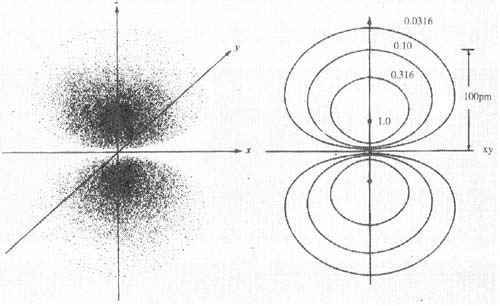
1(ब)2p ऑर्बिटल का इलेक्ट्रॉन समघनत्व रेखा चित्र यह दाअसल एक ठोस मॉडल की आड़ी काट है। प्रत्येक रेखा पर लिखे अंक उस सतह पर इलेक्ट्रॉन पाए जाने की संभाविता के घोतक हैं। यानी पाइकोमीटर =10-12 मीटर। 2. 3pz आर्बिटल का इलेक्ट्रॉन समघनत्व रेखाचित्र।
अब हम हाइड्रोजन के इन दो परमाणुओं को पास-पास लाना शुरू करते हैं। एक हद से पास आने पर ये एक-दूसरे को प्रभावित करने लगते हैं। दोनों के केन्द्रक धनावेशित हैं। वे एक-दूसरे को दूर धकेलेने लगते हैं। दोनों के इलेक्ट्रॉन बादल ऋणावेशित हैं। इसलिए वे भी एक-दूसरे को दूर धकेलेंगे। यान परमाणु पास-पास आने से रोके जांगे- परन्तु साथ में एक परमाणु का केन्द्रक, दूसरे परमाणु के इलेक्ट्रॉन बादल को आकर्षित करने लगता है। वैसे तो हम यह सोचते हैं कि केन्द्रक परमाणु के बीच में है तथा इलेक््रॉन आवेश उसके आसपास है, इसलिए केन्द्रक का प्रभाव बाहर नहीं होना चाहिए। मगर ऐसा होता नहीं है। केन्द्रक का पूरा असर निष्प्रभावी नहीं हो पाता। लिहाज़ा एक परमाणु का केन्द्रक दूसरे परमाणु के इलेक्ट्रॉन बादल को आकर्षित करता है। इस आकर्षण की वजह से दोनों ही परमाणुओं में इलेक्ट्रॉन घनत्व के वितरण की आकृति बदलने लगती है। इलेक्ट्रॉन का घनत्व दोनों केन्द्रकों के बीच बढ़ने लगता है और पूरे तंत्र की ऊर्जा कम होने लगती है।
इलेक्ट्रॉनों के दोनों केन्द्रकों के बीच घनीभूत होने का एक असर और होता है। यह घना इलेक्ट्रॉन-बादल केन्द्रकों के बीच एक पर्दे का काम करता है। अत: केन्द्रकों के बीच विकर्षण का बल थोड़ा कम हो जाता हैहै। अब इस तंत्र को हम हाइड्रोजन का एक अणु कह सकते हैं।
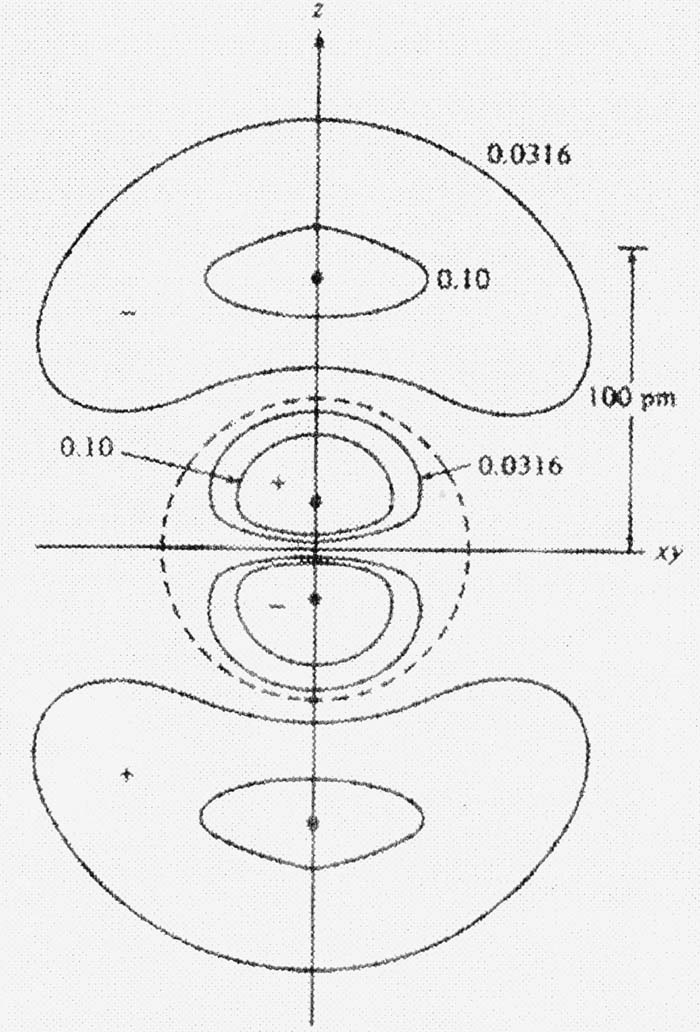
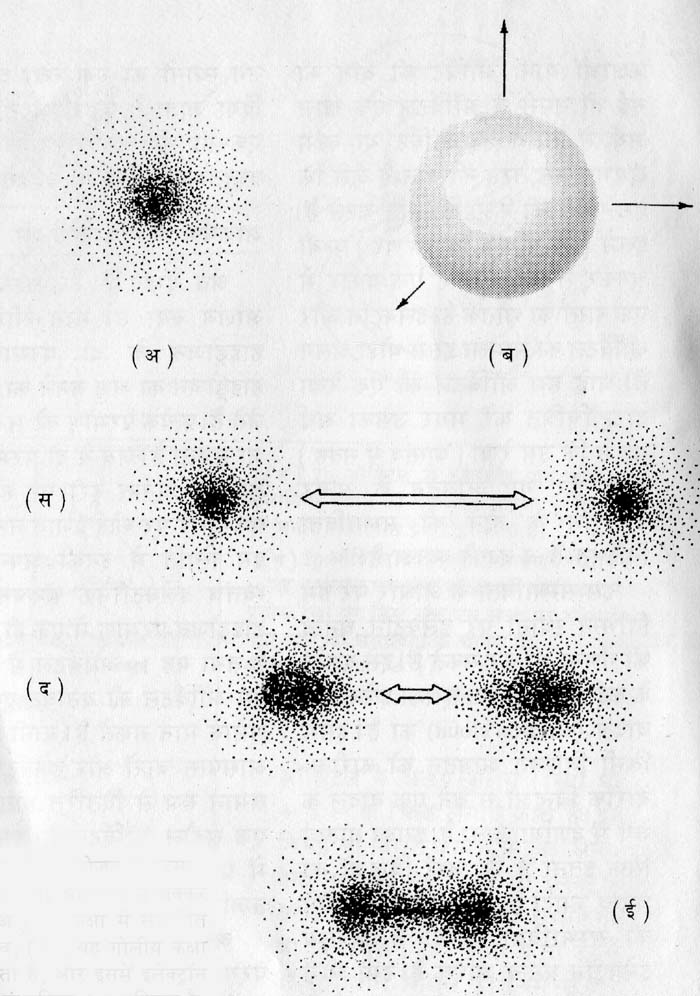 अणु का बनना: हाइड्रोजन के परमाणु का एक इलेक्ट्रॉन, 1 ऑवर्बटल में चक्कर लगाता है। (अ) इस कक्षा में संभावित इलेक्ट्रॉन घनत्व (ब) यह गोलीय कक्षा त्रिआयामी होती है, और इसमें इलेक्ट्रॉन पाए जाने की संभाविता 95 प्रतिशत है; (स) जब दो हाइड्रोजन परमाणु एक दूसरे से पार्याप्त दूरी पर होते हैं तो एक दूसरे पर किसी भी तरह का कोई भी बल नहीं लगाते; (द) जब इनहें पास लाया जाता है तो प्रत्येक परमाणु का इलेक्ट्रॉन संभाविता क्षेत्र दूसरे परमाणु के नाभिक की ओर आकर्षित होना शुरू होता है, और इनका मूल आकार बिगड़ना शुरू होता है। इस वजह से दोनों नाभिकों के बीच वालो क्षेत्र में इलेक्ट्रॉन संभाविता बढ़ती है; (ई) और पास आने पर समान आवेश के ाकरण दोनों नाभिक एक दूसरे को विकर्षित करना भी शुरू कर देते हैं, और एक सीमा आती है कि दोनों पर माणु एक दूसरे के और पास नहीं आ पाते। इस तरह किसी अणु में सहबंध की लंबाई दरअसल दरअसल वह दूरी है जिस पर आकर्षण और विकर्षण बलों में संतुलन बना हुआ है।
अणु का बनना: हाइड्रोजन के परमाणु का एक इलेक्ट्रॉन, 1 ऑवर्बटल में चक्कर लगाता है। (अ) इस कक्षा में संभावित इलेक्ट्रॉन घनत्व (ब) यह गोलीय कक्षा त्रिआयामी होती है, और इसमें इलेक्ट्रॉन पाए जाने की संभाविता 95 प्रतिशत है; (स) जब दो हाइड्रोजन परमाणु एक दूसरे से पार्याप्त दूरी पर होते हैं तो एक दूसरे पर किसी भी तरह का कोई भी बल नहीं लगाते; (द) जब इनहें पास लाया जाता है तो प्रत्येक परमाणु का इलेक्ट्रॉन संभाविता क्षेत्र दूसरे परमाणु के नाभिक की ओर आकर्षित होना शुरू होता है, और इनका मूल आकार बिगड़ना शुरू होता है। इस वजह से दोनों नाभिकों के बीच वालो क्षेत्र में इलेक्ट्रॉन संभाविता बढ़ती है; (ई) और पास आने पर समान आवेश के ाकरण दोनों नाभिक एक दूसरे को विकर्षित करना भी शुरू कर देते हैं, और एक सीमा आती है कि दोनों पर माणु एक दूसरे के और पास नहीं आ पाते। इस तरह किसी अणु में सहबंध की लंबाई दरअसल दरअसल वह दूरी है जिस पर आकर्षण और विकर्षण बलों में संतुलन बना हुआ है।
केन्द्रक ओर इलेक्ट्रॉन के बीच आकर्षण के कारण दोनों परमाणु और भी पास-पास आ जाते हैं और अणु की ऊर्जा और भी कम हो जाती है। मगर यह स्थिति एक निश्चित निकटता तक ही जारी रहेगी। जब केन्द्रक एक हद से ज़्यादा निकट आ जाएंगे तो उनके बीच का विकर्षण इन्हें फिर दूर धकेल देगा। जब दूर हो जाएंगे तो फिर आकर्षण होने लगेगा। यानी अब ये दो परमाणु एक पेण्डुलम की तरह दूर-पास होते रहेंगे- गोया कि किसी स्प्रिंग से आपस में जुड़े हों। इस ‘स्प्रिंग’ की अधिकतम लम्बाई और नयूनतम लम्बाई के बीच एक मध्यमान बिन्दु होता है जहां आकर्षण व विकर्षण के बल एकदम संतुलित होते हैं। इसी को बन्ध–लम्बाई (Bond length) कहते हैं।
हमने ऊपर कहा कि इलेक्ट्रॉन केन्द्रकों के बीच घनीभूत हो गए हैं। इसका मतलब यह है कि इस नए तंत्र में (यानी अणु में) इलेक्ट्रॉन के पाए जाने की सम्भाविता का वितरण बदल गया है। यह वितरण इस तरह बदलता है कि पूरे तंत्र की ऊर्जा कम हो जाती है। मगर सवाल यह है कि इस पूरी अंत:क्रिया व बदले हुए सम्भाविता वितरण को कैसे समझा जाए? इसी बात को समझने के दो तरीके हैं – ‘वेलेन्स बॉण्ड मॉडल’ तथा ‘मॉलाक्यूलर ऑर्बिटल मॉडल’ लेकिन इन पर बातचीत अगली बार।
सुशील जोशी – पर्यावरण एवं विज्ञान लेखन में सक्रिय। होशंगाबाद विज्ञान शिक्षण कार्यक्रम से संबद्ध।