लेखक : उमा सुधीर
अनुवाद : सुशील जोशी [Hindi PDF, 191 kB]
 इस लेख के पिछले भाग में मैंने नाइट्रोजन की टिकाऊ प्रकृति की चर्चा की थी और यह बताने की कोशिश की थी कि आणविक कक्षक का सिद्धांत हमें यह समझने में मदद करता है कि क्यों नाइट्रोजन सामान्यक हालात में अक्रिय होती है। यहां में उसी से सम्बंझधित एक मुददे की चर्चा करूंगी।
इस लेख के पिछले भाग में मैंने नाइट्रोजन की टिकाऊ प्रकृति की चर्चा की थी और यह बताने की कोशिश की थी कि आणविक कक्षक का सिद्धांत हमें यह समझने में मदद करता है कि क्यों नाइट्रोजन सामान्यक हालात में अक्रिय होती है। यहां में उसी से सम्बंझधित एक मुददे की चर्चा करूंगी।
हम जानते हैं कि हवा में एक द्विपरमाणविक अणु के रूप में पाई जाने वाली नाइट्रोजन जीवधारियों में बहुत अहम भूमिका निभाती है। यह कई जैविक रूप से महत्वापूर्ण अणुओं में पाई जाती है, जैसे प्रोटीन्सब, न्यू क्लिक एसिड और अल्केभलॉइड्स। तो ये जीवधारी इस अक्रिय तत्व को कैसे इन अणुओं में जोड़ लेते हैं?
पहले तो यह देखते हैं कि जीवित तंत्रों से बाहर यानी कारखानों में यह काम कैसे किया जाता है।
नाइट्रोजन को उसके यौगिकों में बदलने का सबसे आम तरीका यह अपनाया जाता है कि पहले उसे अमोनिया में बदल दिया जाता है। इसके लिए हैबर प्रक्रिया का उपयोग किया जाता है जिसमें उत्प्रे रक की उपस्थिति में ऊंचे तापमान और दबाव पर नाइट्रोजन की क्रिया हाइड्रोजन से करवाई जाती है :
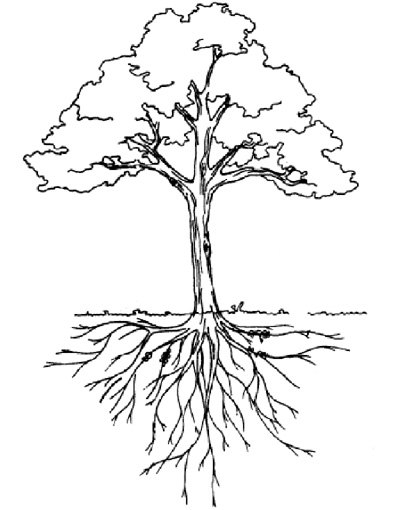
N2 + 3H2 2NH3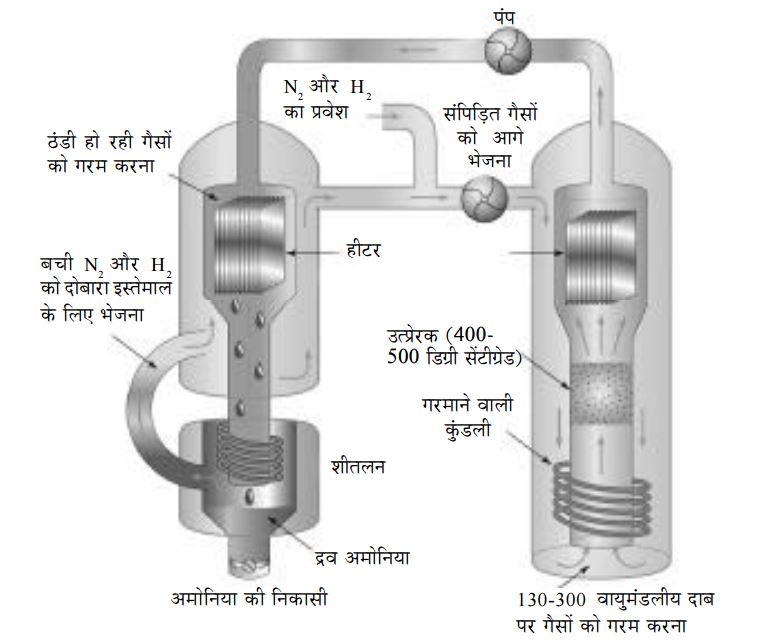 हैबर विधि से अमोनिया बनाना – वैज्ञानिक काफी पहले जान गए थे कि नाइट्रोजन और हाइड्रोजन के मिश्रण को विद्युत स्पा र्क से गुज़ारा जाए तो अमोनिया निर्मित होती है और यह क्रिया उल्टाीई भी जा सकती है। लेकिन इस तरह से बेहद कम मात्रा में अमोनिया बनती थी।
हैबर विधि से अमोनिया बनाना – वैज्ञानिक काफी पहले जान गए थे कि नाइट्रोजन और हाइड्रोजन के मिश्रण को विद्युत स्पा र्क से गुज़ारा जाए तो अमोनिया निर्मित होती है और यह क्रिया उल्टाीई भी जा सकती है। लेकिन इस तरह से बेहद कम मात्रा में अमोनिया बनती थी।
हैबर ने 1913 में जो विधि अपनाई उसमें उत्प्रेटरकों का सहारा लिया। इस विधि में तापमान लगभग 600 डिग्री सेंटीग्रेड तथा दबाव 200 वायुमंडलीय दाब तक होता था। इस तरीके में शुरूआत में ली गई हाइड्रोजन और नाइट्रोजन से मात्र 8 प्रतिशत अमोनिया प्राप्ती होती थी।
मौजूदा समय में हैबर विधि में किए गए सुधारों को वज़ह से उपयोग में लाई गई गैसों से करीब 40 से 60 प्रतिशत अमोनिया प्राप्ति होती है। इसमें उत्प्रेंरक के रूप में सरंध्र लोहे और पोटेशियम एल्यु मिनियम के ऑक्साेइड का इस्ते्माल होता है और तापमान भी अपेक्षाकृत रूप से कम होता है।
यहां ऊपर दिए चित्र में हैबर विधि का एक संशोधित रूप है, जिसमें दिखाया गया है कि किस तरह विविध प्रक्रियाओं से होकर गुज़रते हुए हाइड्रोजन और नाइट्रोजन से तरल अमोनिया प्राप्त होती है।
यह क्रिया 5500 से. तापमान, 200 वायुमंडल दबाव और थोड़े सीरियम व क्रोमियम मिले लौह ऑक्सापइड उत्प्रेयरक को उपस्थिति में होती है। उत्प्रेमरक उन पदार्थों को कहते हैं जो किसी रासायनिक अभिक्रिया की रफ्तार बढ़ाते हैं।
यह क्रिया उत्क्र मणीय (reversible) है और इसमें अमोनिया की उपज बढ़ाने के लिए अमोनिया को क्रिया के स्थाफन से हटाते जाते हैं। इस मूल प्रक्रिया में धीरे-धीरे कई संशोधन किए गए हैं। जैसे आजकल इसमें कहीं ज़्यादा दबाव का उपयोग किया जाता है। इसके अलावा, अमोनिया को लगातार यहां से हटाया जाता है और नाइट्रोजन व हाइड्रोजन का रिसायक्ंलग किया जाता है।
हैबर अभिक्रिया को देखकर ही स्पाष्ट हो जाता है कि नाइट्रोजन की क्रिया करवाना हंसी-खेल नहीं है। इसलिए बहुत अधिक तापमान व दबाव ज़रूरी होते हैं। मगर सजीव ऐसे ऊंचे तापमान और दबाव के बिना भी इस प्रक्रिया को अंजाम देते हैं। इसलिए यह सवाल महत्ववपूर्ण हो जाता है कि सजीव इस अक्रिय तत्वा को यौगिकों में कैसे बदलते हैं।
प्रकृति के ढंग निराले
प्रकृति में नाइट्रोजन को उसके यौगिकों में बदलने की यही प्रक्रिया सजीव और निर्जीव दोनों रास्तों से होती रहती है। दूसरे वाले रास्ते से यह प्रक्रिया बिजली कड़कने के समय होती है। इस दौरान नाइट्रोजन के ऑक्सा्इड्स बन जाते हैं और ये बारिश के पानी में घुलकर मिट्टी में पहुंच जाते हैं। बिजली कड़कना एक ऐसी
|
क्रिया की रफ्तार किसी भी क्रिया की रफ्तार बढ़ाने के दो ही तरीके हो सकते हैं। पहला तरीका यह है कि ऐसी स्थितियां निर्मित की जाएं कि अभिकारक (Reactant) के अणु आपस में ज़्यादा बार टकराएं। इससे उनके बीच क्रिया होने की संभावना बढ़ जाती है। तापमान या दबाव बढ़ाकर हम मूलत: टक्केरों की संख्या बढ़ा देते हैं। जब विघटन क्रिया करवानी हो, तो टक्क रों की संख्या कम भी करनी पड़ सकती है। |
उग्र घटना है। अर्थात प्रकिृति में भी नाइट्रोजन उग्र महौल में ही क्रिया करती है।सजीव जगत में इस प्रक्रिया को कुछ बैक्टीीरिया संपादित करते हैं। इन्हेंस नाइट्रोजन स्थिर करने वाले बैक्टी रिया कहते हैं। जैसे राइज़ोबियम। ये सामान्यट परिस्थितियों (वायुंडलीय दबाव और 20-37 डिग्री सेल्सियस तापमान) पर इस कार्य को अंजाम देते हैं।
नाइट्रोजन से अमोनिया बनाने की इन दो विधियों – हैबर विधि और बैक्टीऔरिया विधि- की तुलना करें तो हैरत होती है। आखिर ऐसा क्योंि है कि सजीवों के लिए नाइट्रोजन के टिकाऊ अणु को तोड़ना इतना सहज है जबकि
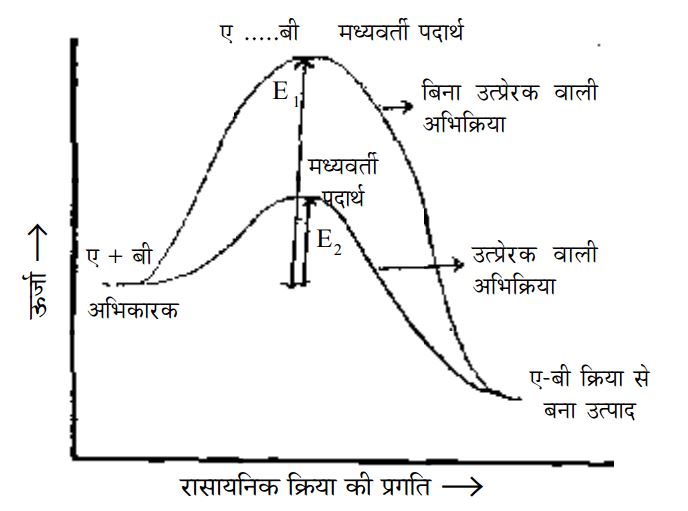 रासायनिक क्रिया की प्रगति
रासायनिक क्रिया की प्रगति
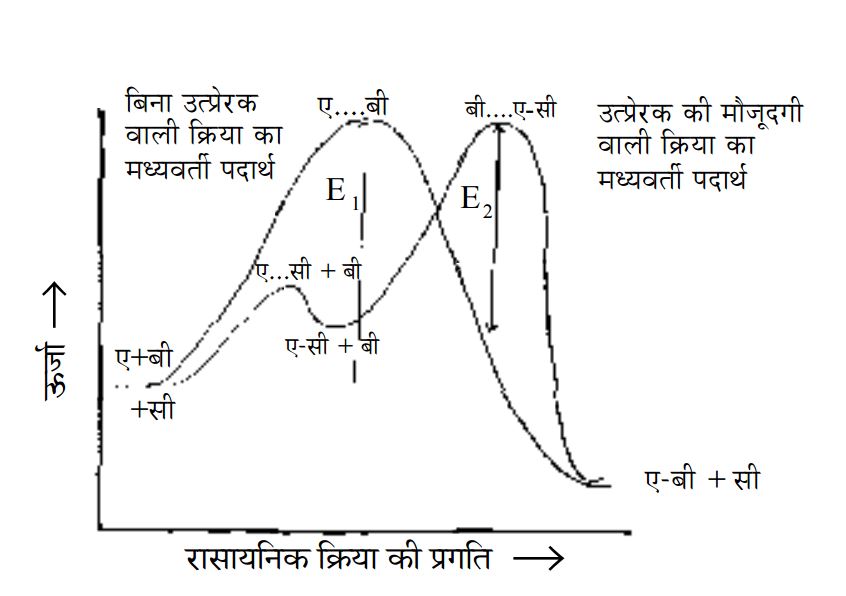
E1 बिना उत्प्र्रेक वाली रासायनिक क्रिया के लिए सक्रियकरण ऊर्जा
E2 उत्प्रे्रक वाली रासायनिक क्रिया के लिए सक्रियकरण ऊर्जा
चित्र- 1 कई क्रियाओं में उत्पाकद को कुल ऊर्जा स्थिति अभिकारकों से नीचे यानी कम होती है परन्तु फिर भी ये अभिक्रियाएं अपने आप आसानी से नहीं हो पाती क्योंकि क्रिया के दौरान जो मयध्ययवर्ती पदार्थ बनता है उसकी ऊर्जा स्थिति काफी ऊंची है। अभिकारकों को मध्यरवर्ती पदार्थ में दबलने के लिए जो ऊर्जा देनी पड़ती है उसे सक्रियकरण ऊर्जा कहते हैं। यानी इन क्रियाओं में सक्रियकरण ऊर्जा (E1) काफी ज़्यादा होती है। इसलिए इन्हेंर संभव बनाने के लिए विशेष परिस्थितियों की ज़रूरत होती है।
अगर इन क्रियाओं में उत्प्रे रक के रूप में एंज़ाइम इस्तेकमाल किए जाएं तो जो मध्यलवर्ती पदार्थ बनता है उसकी सक्रियकरण ऊर्जा (E2) काफी कम हो जाती है। इस वजह से अब यह क्रिया सामान्यज परिस्थितियों में भी संभव हो पाती है।
कोशिका के बाहर हमें भारी दबाव और अत्यंयत ऊंचे तापमान का सहारा लेना पड़ता है? देखा जाए तो सजीवों में यह सहजता सिर्फ नाइट्रोजन स्थिरीकरण के मामले में ही नहीं दिखती। ऐसी कई क्रियाएं हैं जो कोशिाकाओं में सहजता से होती हैं मगर प्रयोगशाला में करवाने के लिए खूब पापड़ बेलने पड़ते हैं। इस चमत्काकरिक सहजता का राज़ एंज़ाइमों की संरचना व सक्रिय बिंदुओं में छिपा है।
बैक्टींरिया द्वारा नाइट्रोजन को अमोनिया में बदला जाना अत्यंत महत्वतपूर्ण क्रिया है क्योंंकि इसी के ज़रिए नाइट्रोजन को सजीव तंत्र में समाहित किया जाता है। इस क्रिया को बैक्टीारिया द्वारा उत्पतन्नव नाइट्रोजिनेस नामक एक एंज़ाइम संपन्नो करता है। नाइट्रोजिनेस की क्रिया को समझने से पहले यह देखते हैं कि आम तौर पर सजीव तंत्रों में होने वाली क्रियाओं में एंज़ाइमों की भूमिका क्यान होती है।
एंज़ाइम
एंज़ाइम जैविक उत्प्रे रक हैं। ये मुख्यात: प्रोटीन्सत होते हैं। (देखिए चित्र -1)
मान लीजिए A और B पदार्थो की क्रिया से A B बनता है। इस क्रिया की समफलता के लिए ज़रूरी है कि दोनों अभिकारक सही कोण से पास-पास आएं (टकराएं) और सही तरीके से जुड़ जाएं।
कभी-कभी क्रिया पूरी होने से पहले एक मध्यटवर्ती पदार्थ बनता है जिसकी ऊर्जा अभिकारकों व उत्पा द दोनों से अधिक होती है। यह मध्यावर्ती पदार्थ फिर अंतिम पदार्थ (जिसे एक्टिवेट्ड कॉम्पकलेक्सा या सक्रिय संकुल भी कहा जाता है) तक पहुंचने के लिए अभिकारकों को जितनी ऊर्जा की ज़रूरत होती है, उसे सक्रियकरण ऊर्जा को कम कर देते हैं। ऊर्जा की ज़रूरत कम करने के लिए वे अभिकारकों को आपस में जोड़ने का एक वैकल्पिक मार्ग उपलब्धि करा देते हैं- A पहले उत्प्रे रक/एंज़ाइम C से जुड़ता है, फिर यह एंज़ाइम-अभिकारक संकुल क्रिया को पूरा करता है। एंज़ाइम द्वारा वैकल्पिक अल्पआ ऊर्जा मार्ग कई तरह से उपलब्ध् करवाया जा सकता है:
|
शुरुआती पदार्थ से अंतिम पदार्थ जब कोई भी अभिक्रिया होती है, तो उसमें शुरुआती पदार्थ (अभिकारक) और अंतिम (उत्पा)द) के बीच ऊर्जा का अंतर होता है। यदि अभिकारकों की कुल ऊर्जा उत्पाीदों की कुल ऊर्जा से अधिक है तो अक्सतर यह क्रिया अनायास ही होती रहेगी। दूसरी ओर, यदि अभिकारकों की कुल ऊर्जा उत्पािदों से कम है तो क्रिया को करवाने के लिए ऊर्जा देनी पड़ेगी। इसमें कुछ जटिलताएं भी होती हैं। जैसे प्राय: अभिकारक सीधे उत्पाकद में तब्दी ल नहीं होते – पहले एक मध्यंतर्वी पदार्थ बनता है, जो बाद में उत्पा द में तब्दी्ल होता है। ऐसी अभिक्रियाओं में यह भी देखना होता है कि ऊर्जा के हिसाब से मध्य्वर्ती पदार्थ कहां स्थित है। आम तौर पर अभिकारकों को मध्यतवर्ती पदार्थ में बदलने के लिए ऊर्जा देनी पड़ती है। इसे सक्रियकरण ऊर्जा (Activation Energy) कहते हैं। |
E1 बिना उत्प्रतरेक वाली रासायनिक क्रिया के लिए सक्रियकरण ऊर्जा
E2 उत्प्रे्रक वाली रासायनिक क्रिया के लिए सक्रियकरण ऊर्जा
चित्र-2 : कुछ क्रियाओं में जब अभिकारक एंज़ाइम से जुड़ता है तो उसको त्रिआयामी संरचना बदलकर एक उच्चकतर ऊर्जा वाली स्थिति में आ जाती है। इसमें भी एंज़ाइम सी की वजह से क्रिया की सक्रियकरण ऊर्जा (E2) कम हो जाती है। इस चित्र में उत्प्रेकरक/एंज़ाइम सी की मौजूदगी में ऐसी ही एक अभिक्रिया दिखाई गई है।
1. दोनों अभिकारक एंज़ाइम के सक्रिय बिंदु पर पास-पास जुड़ सकते हैं जिससे क्रिया की रफ्तार बढ़ जाती है। इसका मतलब यह है कि क्रिया करने वाले दोनों पदार्थों को एक ही समय पर एक स्थाकन पर पहुंचने की ज़रूरत खत्मय हो जाती है। यदि एक पदार्थ पहले पहुंचा तो यह एंज़ाइम से जुडकर स्थिर हो जाएगा। अब दूसरा पदार्थ जब भी आएगा, पहला पदार्थ उसका इंतज़ार करता मिलेगा। दरअसल एंज़ाइम का प्रोटीन अणु काफी विशाल होता है। केवल इसका एक छोटा सा हिस्साै ही उत्प्रे रण यानी केटेलिसिस में हिस्साा लेता है। अणु का शेष भाग इस सक्रिय हिस्सेा यानी सक्रिय बिन्दुप को विशेष आकृति में बनाए रखता है।
2. अभिकारक जब एंज़ाइम से जुड़ते हैं तो उनका विशेष उन्मुसखीकरण (orientation) नाइट्रोजिनेस बन जाता है जिससे उनके बीच क्रिया होने में सुविधा होती है।
3. एंज़ाइम अम्ला या क्षार की तरह कार्य करते हुए भी क्रिया को गति दे सकते हैं। जैसे किसी एंज़ाइम में अम्लीहय या क्षारीय साइड- श्रृंखला (site-chain) जुड़ी होती है। ये श्रंखलाएं घोल में उपस्थित अम्लआ या क्षार की अपेक्षा क्रिया में बेहतर ढंग से सहयोग कर पाती हैं क्यों कि ये सक्रिय बिन्दुओं पर जुड़े अभिकारकों के नज़दीक ही होती हैं।
4. जब अभिकारक एंज़ाइम से जुड़ता है तो कई बार उसकी त्रिआयामी संरचना इस तरह बदलती है कि वह एक उच्त्जब र ऊर्जा वाली स्थिति में आ जाती है। क्रिया के सक्रिय संकुल बनने के लिए यह स्थिति ज़रूरी होती है। इस मामले में क्रिया का ऊर्जा चित्र कुछ इस प्रकार का होता है (देखिए चित्र -2)।
ऐसे मामलों में रासायनिक क्रिया शायद इसलिए तेज़ हो जाती है क्योंोकि अभिकारक-एंज़ाइम संकुल की ऊर्जा अकेले अभिकारक से अधिक होती है। इसलिए सक्रियकरण ऊर्जा की ज़रूरत कम हो जाती है।
दरअसल किसी भी क्रिया में शुरूआती अभिकारको और अंतिम उत्पाजद के बीच कुल ऊर्जा परिवर्तन में तो कोई फेरबदल नहीं होता मगर एंज़ाइम के होने से यह ऊर्जा परिवर्तन चरणों में संभव हो जाता है।
कुल मिलाकर सामान्यत स्थिति में अभिकारकों के बीच अनगिनत बेतरतीब टक्कोरों में वह बात नहीं बन पाती जो एंज़ाइम की उपस्थिति में आसानी से बन जाती है। एंज़ाइम अभिकारकों से जुड़ जाता है, उन्हेंत परस्पजर सही दिशा में जमा देता है, ज़रूरत के अनुसार अम्ली य या क्षारीय परिवेश उपलब्धह करा देता है, और इस तरह से यह सुनिश्चित करता है कि क्रिया एक निर्धारित ढंग से चले। एंज़ाइम न हो तो ये सारी ज़रूरी बातें- उन्मुाखीकरण, ऊर्जा, हाइड्रोजन आयन सांद्रता – संयोग के भरोसे रहती हैं।
नाइट्रोजिनेस
तो नाइट्रोजन स्थिरिकरण पर लौटे। इस क्रिया के लिए एंज़ाइम है नाइट्रोजिनेस जो वायुमंडल की नाइट्रोजन को अमोनिया में बदल देता है। यह अमोनिया फिर सजीव तंत्र में समाहित हो जाती है। मज़ेदार बात है कि तथाकथित विकसित पेड़-पौधेां और जंतुओं में नाइट्रोजन स्थिरीकरण की क्षमता नहीं होती। वायुमंडल की नाइट्रोजन को कैद करना तो राइज़ोबियम और क्लोंस्ट्रिडियम जैसे बैक्टीतरिया के जि़म्मे है।ये बैक्टीडरिया सहजीवी हैं। गैर-सहजीवी परिस्थिति में नाइट्रोजन स्थिरीकरण का काम नीली-हरी शैवाल, मिट्टी में रहने वाले एज़ोटोबैक्टजर के अलावा क्लेसबसिएला और एक्रोमोबैक्ट्र जैसे कुछ बैक्टीजरिया द्वारा किया जाता है। प्रकाश संश्लेोषण करने वाले सारे बैक्टीजरिया भी नाइट्रोजन स्थिरीकरण कर सकते हैं। इन बैक्टीटरिया को मेहनत का फल पेड़-पौधों को मिलता है और उनके ज़रिए जंतुओं को। इस सहजीवी संबंध में फायदा बैक्टिरिया को भी होता है कि उन्हेंि बैठे बिठाए भोजन मिलता है।
|
कितनी ऊर्जा खर्च होती है 1. नाइट्रोजिनेस एंज़ाइम संकुल नाइट्रोजन के एक अणु को हाइड्रोजन से जोड़कर अमोनिया के दो अणु बनाने में 12 एटीपी अणुओं (कोशिकाओं की ऊर्जा मुद्रा) के बराबर ऊर्जा खर्च करता है। इसके अलावा बचे हाइड्रोजन आयनों को हाइड्रोजन में बदलने में एटीपी 4 और अणु खर्च होते हैं। पूरी क्रिया निम्नाडनुसार हैं: |
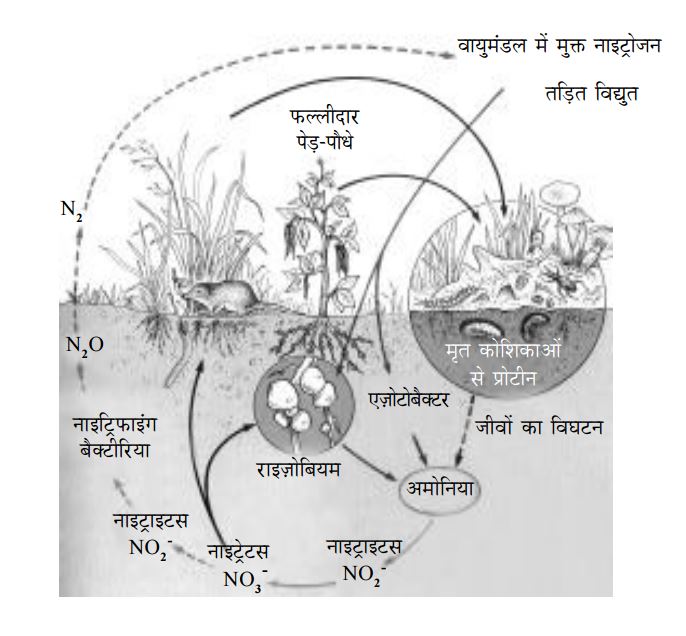
नाइट्रोजन चक्र में वायुमंडल की नाइट्रोजन को अमोनिया, नाइट्रेट व नाइट्राइट्स में बदला जाता है, जिसे विकसित वनस्पतियां ग्रहण करके विभिन्न अमोनो अम्लों और अन्य नाइट्रोजन युक्त कार्बनिक पदार्थों में बदलती हैं। इसका उपभोग जंतु करते हैं। जब पेड़-पौधे और जंतु मरते हैं तब विभिन्न बैक्टीरिया नाइट्रोजन युक्त जटिल अणुओं को तोड़-तोड़कर वापस अमोनिया, नाइट्राइट्स और नाइट्रेट्स में बदल देते हैं। कुछ अन्य बैक्टीरिया इन पदार्थों को वापस नाइट्रोजन में भी बदल डालते हैं। इस प्रकार से नाइट्रोजन सजीव तंत्र में अंगीकार होती और फिर से मुक्त हो जाती है। यही नाइट्रोजन चक्र है।
नाइट्रोजिनेस एंज़ाइम संकुल, दो प्रोटीन्सा का संकुल होता है। इनमें से एक लौह प्रोटीन है और दूसरा लौह-मॉलिब्डेिनम प्रोटीन है। इनमें से कोई भी अकेला कार्य नहीं कर सकता है। नाइट्रोजन स्थिरीकरण की क्रिया तभी होती है जब ये दोनों प्राटीन्सइ मौजूद हों। एक प्रोटीन न हो तो दूसरा अपने बल पर मध्यीवर्ती पदार्थ का निर्माण नहीं कर पाता। यह एंज़ाइम संकुल नाइट्रस ऑक्सा इड, एसिटिलीन, एज़ाइड, साएनाइड व अन्यं सम्बंरधित पदार्थों का अवकरण (reduction) भी कर सकता है।
इसकी क्रियाविधि के बारे में सोचा जाता है कि NN को चरणबद्ध ढंग से डाईइमाइड NH=NH में और फिर हाइड्रेज़ीन NH2-NH2 में और अंतत: 2NH3 में बदला जाता है। मगर रोचक तथ्यफ यह है कि यह एंज़ाइम संकुल इनमें से किसी भी अभिकारक पर सीधे क्रिया नहीं करता। यानी यदि नाइट्रोजन की बजाए डाईइमाइड अथवा हाइड्रेज़ीन दिए जाएं तो यह एंज़ाइम उन्हेंन अमोनिया में तब्दीजल नहीं कर पाता। इससे पता चलता है कि ये वास्तेविक मध्ययवर्ती पदार्थ नहीं हैं। या यह हो सकता है कि एंज़ाइम के सक्रिय बिंदु इन मध्योवर्तियों को सीधे लेकर अमोनिया नहीं बना सकते। हो सकता है कि एंज़ाइम के सक्रिय बिंदु विशिष्टं रूप से मात्र नाइट्रोजन के अणु से ही जुड़ पाते हैं।
|
सहजीवी बैक्टीरिया वायुमंडल से नाइट्रोजन ले सकने वाले अधिकांश जीव स्वतंत्र जीवी हैं। अलबत्ता, कुछ जीव ऐसे भी हैं जो फलीदार पौधों (Legumes) के साथ सहजीवी सम्बंध में बंध गए हैं। इन सहजीवी बैक्टीरिया की मदद से नाइट्रोजन स्थिरीकरण का काम जहां फलीदार पौधों की 13,000 से ज़्यादा प्रजातियों में होता है, वहीं गैर-फलीदार पौधों की 250 प्रजातियां ही इस काम को कर पाती हैं। गैर-फलीदार पौधों के साथ जुड़े बैक्टिरिया उनके तनों व पत्तियों पर पाए जाते हैं; जड़ों पर गठानें मात्र फलीदार पौधों में ही पाई जाती हैं। ये बैक्टीरिया फलीदार पौधों की जड़ों पर गठानें बनाकर रहते हैं और नाइट्रोजन स्थिरीकरण के लाभ के बदले में उनकी शेष ज़रूरतें फलीदार पौधा पूरी करता है। |
अकेले के बस की बात नहीं
नाइट्रोजिनेस के साथ सम्बनद्ध एक और एंज़ाइम लेगहिमोग्लोनबीन है जो फलीदार पौधेां में उसके काम में मदद करता है। यह हमारे खून में मौजूद हिमोग्लोंबीन से मिलता-जुलता है। इसी की वजह से फलीदार पौधेां की जुड़ों की गठानों में हल्कीम गुलाबी रंगत होती है और इसीलिए इसका नाम लेग-हिमोग्लोाबीन (Leg-haemoglobin) है (फलीदार पौधों को अंग्रेज़ी में लेग्यूइम कहते हैं)। इस एंज़ाइम का काम नाइट्रोजिनेस के आसपास से ऑक्सीठजन को हटाना हे। ऑक्सींजन की उपस्थिति में नाइट्रोजिनेस निष्क्रिय हो जाता है। इससे लगता है कि यह एंज़ाइम सूदूर अतीत में तब विकसित हुआ होगा जब पृथ्वीट के वायुमंडल में ऑक्सीइजन न के बराबर थी और अनॉक्सीा जीवन ही प्रमुख था। लेग-हिमोग्लोटबीन ऑक्सींजन से जुड़ जाता है और उसे नाइट्रोजिनेस संकुल के पास नहीं फटकने देता इस तरह से नाइट्रोजिनेस संकुल की अखंडता बनी रहती है। दूसरी बात यह है कि लेग-हिमोग्लोाबीन का उत्पाेदन सहजीवी बैक्टी रिया द्वारा नहीं बल्कि मेज़बान यानी फलीदार पौधे द्वारा किया जाता है जैसे कि मूंगफली, चना, मटर, मैथी आदि में सहयोग की यह तस्वीार दिखाई देती है।
रास्तेद और भी हैं
सजीव तंत्रों में नाइट्रोजन को नाइट्राइट और नाइट्रेट का निर्माण नाइट्रोसोमोनास और नाइट्रोबैक्टैर जैसे कुछ बैक्टींरिया करते हैं। ये बैक्टीटरिया मिट्टी में उपस्थित अमोनिया का ऑक्सीरकरण करके स्वेयं के लिए ऊर्जा प्राप्तत करते हैं और मिट्टी में नाइट्राइट व नाइट्रेट तैयार कर देते हैं। इस प्रक्रिया को नाइट्रीकरण करहते हैं। इसका परिणाम यह होता है कि विकसित पौधों को मिट्टी में नाइट्रोजन प्रमुख रूप से नाइट्रेट के रूप में मिलती हैहै। कुछ बैक्टी रिया नाइट्रेट को वापस नाइट्रोजन में परिवर्तित कर देते हैं और इस प्रकार से प्रकृति में नाइट्रोजन चक्र चलता रहता है।
तो, हमने देखा कि सजीव तंत्र में नाइट्रोजन जैसे अक्रिय अणु से क्रिया करवाकर जीवन के लिए ज़रूरी अणु पैदा करने के लिए एक पेचीदा व्यजवस्थां बनी है। दरअसल, सजीवों में हर रासायनिक क्रिया के नियंत्रण व समन्वकय हेतु ऐसी ही विस्तृसत प्रणालियां हैं। इन सारी जटिल प्रक्रियाओं का ताना-बाना जब कामकाजी जीवों का रूप देता है तो वाह कहने को जी करता है।
उमा सुधीर : एकलव्यस के विज्ञान शिक्षण कार्यक्रम से संबद्ध हैं। इंदौर में रहती हैं। अनुवाद एवं संपादन: सुशील जोशी: एकलव्यप द्वारा प्रकाशित स्रोत फीचर सेवा से जुड़े हैं।